Сколько равна лямбда воды
Изобретению уже известного вам жидконаполненного калориметра (см. § 06-в) предшествовало создание в ХVIII веке французами П.Лапласом и А.Лавуазье ледяного калориметра. Если при пользовании первым калориметром измеряют изменение температуры жидкости, то при пользовании вторым калориметром измеряют массу растаявшего льда. В ХVIII веке только так и можно было поступить, так как не было общепринятых методов измерения температуры.
Лаплас и Лавуазье опирались на труды своих предшественников, шотландца Д.Блэка и голландца И.Вильке, которые решили ввести в физику новое понятие: скрытая теплота.
Усилиями физиков конца XVIII–начала XIX веков установлено, что количество теплоты прямо пропорционально массе расплавившегося вещества или массе испарившейся жидкости. То есть во сколько раз больше масса вещества, которое перешло в другое состояние, во столько же раз больше нужно теплоты.
Далее показан современный вид формул для расчёта теплоты плавления и теплоты парообразования. Они, наряду с уже известной вам основной калориметрической формулой Q = cmΔt°, по сей день лежат в основе всех методов калориметрических измерений.
Количество теплоты, необходимое для плавления, зависит от массы плавящегося вещества и удельной теплоты плавления:
Q – количество теплоты, Дж
λ – удельная теплота плавления, Дж/кг
m – масса вещества, кг
Точные калориметрические измерения и опыты показывают, что при кристаллизации вещества (это процесс, обратный плавлению) выделяется такое же количество теплоты, какое было затрачено на образование расплава. Это – проявление закона сохранения энергии.
Количество теплоты, необходимое для парообразования, зависит от массы испаряющегося вещества и удельной теплоты парообразования:
Q – количество теплоты, Дж
r – удельная теплота парообразования, Дж/кг
m – масса вещества, кг
Точные калориметрические измерения и опыты показывают, что при конденсации вещества (это процесс, обратный парообразованию) выделяется такое же количество теплоты, какое было затрачено на образование пара. Это – проявление закона сохранения энергии.
Удельные теплоты плавления или парообразования показывают количество теплоты, которое необходимо для плавления или превращения в пар 1 кг вещества при постоянной температуре.

Рассмотрены физические свойства воды: плотность воды, теплопроводность, удельная теплоемкость, вязкость, число Прандтля и другие. Свойства представлены при различных температурах в виде таблиц.
Плотность воды в зависимости от температуры
Принято считать, что плотность воды равна 1000 кг/м 3 , 1000 г/л или 1 г/мл, но часто ли мы задумываемся при какой температуре получены эти данные?
Максимальная плотность воды достигается при температуре 3,8…4,2°С. В этих условиях точное значение плотности воды составляет 999,972 кг/м 3 . Такая температурная зависимость плотности характерна только для воды. Другие распространенные жидкости не имеют максимума плотности на этой кривой — их плотность равномерно снижается по мере роста температуры.
Вода существует как отдельная жидкость в диапазоне температуры от 0 до максимальной 374,12°С — это ее критическая температура, при которой исчезает граница раздела между жидкостью и водяным паром. Значения плотность воды при этих температурах можно узнать в таблице ниже. Данные о плотности воды представлены в размерности кг/м 3 и г/мл.
В таблице приведены значения плотности воды в кг/м 3 и в г/мл (г/см 3 ), допускается интерполяция данных. Например, плотность воды при температуре 25°С можно определить, как среднее значение от величин ее плотности при 24 и 26°С. Таким образом, при температуре 25°С вода имеет плотность 997,1 кг/м 3 или 0,9971 г/мл.
Значения в таблице относятся к пресной или дистиллированной воде. Если рассматривать, например, морскую или соленую воду, то ее плотность будет выше — плотность морской воды равна 1030 кг/м 3 . Плотность соленой воды и водных растворов солей можно узнать в этой таблице.
| t, °С | ρ, кг/м 3 | ρ, г/мл | t, °С | ρ, кг/м 3 | ρ, г/мл | t, °С | ρ, кг/м 3 | ρ, г/мл |
|---|---|---|---|---|---|---|---|---|
| 0 | 999,8 | 0,9998 | 62 | 982,1 | 0,9821 | 200 | 864,7 | 0,8647 |
| 0,1 | 999,8 | 0,9998 | 64 | 981,1 | 0,9811 | 210 | 852,8 | 0,8528 |
| 2 | 999,9 | 0,9999 | 66 | 980 | 0,98 | 220 | 840,3 | 0,8403 |
| 4 | 1000 | 1 | 68 | 978,9 | 0,9789 | 230 | 827,3 | 0,8273 |
| 6 | 999,9 | 0,9999 | 70 | 977,8 | 0,9778 | 240 | 813,6 | 0,8136 |
| 8 | 999,9 | 0,9999 | 72 | 976,6 | 0,9766 | 250 | 799,2 | 0,7992 |
| 10 | 999,7 | 0,9997 | 74 | 975,4 | 0,9754 | 260 | 783,9 | 0,7839 |
| 12 | 999,5 | 0,9995 | 76 | 974,2 | 0,9742 | 270 | 767,8 | 0,7678 |
| 14 | 999,2 | 0,9992 | 78 | 973 | 0,973 | 280 | 750,5 | 0,7505 |
| 16 | 999 | 0,999 | 80 | 971,8 | 0,9718 | 290 | 732,1 | 0,7321 |
| 18 | 998,6 | 0,9986 | 82 | 970,5 | 0,9705 | 300 | 712,2 | 0,7122 |
| 20 | 998,2 | 0,9982 | 84 | 969,3 | 0,9693 | 305 | 701,7 | 0,7017 |
| 22 | 997,8 | 0,9978 | 86 | 967,8 | 0,9678 | 310 | 690,6 | 0,6906 |
| 24 | 997,3 | 0,9973 | 88 | 966,6 | 0,9666 | 315 | 679,1 | 0,6791 |
| 26 | 996,8 | 0,9968 | 90 | 965,3 | 0,9653 | 320 | 666,9 | 0,6669 |
| 28 | 996,2 | 0,9962 | 92 | 963,9 | 0,9639 | 325 | 654,1 | 0,6541 |
| 30 | 995,7 | 0,9957 | 94 | 962,6 | 0,9626 | 330 | 640,5 | 0,6405 |
| 32 | 995 | 0,995 | 96 | 961,2 | 0,9612 | 335 | 625,9 | 0,6259 |
| 34 | 994,4 | 0,9944 | 98 | 959,8 | 0,9598 | 340 | 610,1 | 0,6101 |
| 36 | 993,7 | 0,9937 | 100 | 958,4 | 0,9584 | 345 | 593,2 | 0,5932 |
| 38 | 993 | 0,993 | 105 | 954,5 | 0,9545 | 350 | 574,5 | 0,5745 |
| 40 | 992,2 | 0,9922 | 110 | 950,7 | 0,9507 | 355 | 553,3 | 0,5533 |
| 42 | 991,4 | 0,9914 | 115 | 946,8 | 0,9468 | 360 | 528,3 | 0,5283 |
| 44 | 990,6 | 0,9906 | 120 | 942,9 | 0,9429 | 362 | 516,6 | 0,5166 |
| 46 | 989,8 | 0,9898 | 125 | 938,8 | 0,9388 | 364 | 503,5 | 0,5035 |
| 48 | 988,9 | 0,9889 | 130 | 934,6 | 0,9346 | 366 | 488,5 | 0,4885 |
| 50 | 988 | 0,988 | 140 | 925,8 | 0,9258 | 368 | 470,6 | 0,4706 |
| 52 | 987,1 | 0,9871 | 150 | 916,8 | 0,9168 | 370 | 448,4 | 0,4484 |
| 54 | 986,2 | 0,9862 | 160 | 907,3 | 0,9073 | 371 | 435,2 | 0,4352 |
| 56 | 985,2 | 0,9852 | 170 | 897,3 | 0,8973 | 372 | 418,1 | 0,4181 |
| 58 | 984,2 | 0,9842 | 180 | 886,9 | 0,8869 | 373 | 396,2 | 0,3962 |
| 60 | 983,2 | 0,9832 | 190 | 876 | 0,876 | 374,12 | 317,8 | 0,3178 |
Следует отметить, что при увеличении температуры воды (выше 4°С) ее плотность уменьшается. Например, по данным таблицы, плотность воды при температуре 20°С равна 998,2 кг/м 3 , а при ее нагревании до 90°С, величина плотности снижается до значения 965,3 кг/м 3 . Удельная масса воды при нормальных условиях значительно отличается от ее плотности при высоких температурах. Средняя плотность воды, находящейся при температуре 200…370°С намного меньше ее плотности в обычном температурном диапазоне от 0 до 100°С.
Смена агрегатного состояния воды приводит к существенному изменению ее плотности. Так, величина плотности льда при 0°С имеет значение 916…920 кг/м 3 , а плотность водяного пара составляет величину в сотые доли килограмма на кубический метр. Следует отметить, что значение плотности воды почти в 1000 раз больше плотности воздуха при нормальных условиях.
Кроме того, вы также можете ознакомиться с таблицей плотности веществ и материалов.
Физические свойства воды при температуре от 0 до 100°С
В таблице представлены следующие физические свойства воды: плотность воды ρ, удельная энтальпия h, удельная теплоемкость Cp, теплопроводность воды λ, температуропроводность воды а, вязкость динамическая μ, вязкость кинематическая ν, коэффициент объемного теплового расширения β, коэффициент поверхностного натяжения σ, число Прандтля Pr. Физические свойства воды приведены в таблице при нормальном атмосферном давлении в интервале от 0 до 100°С.
Физические свойства воды существенно зависят от ее температуры. Наиболее сильно эта зависимость выражена у таких свойств, как удельная энтальпия и динамическая вязкость. При нагревании значение энтальпии воды значительно увеличивается, а вязкость существенно снижается. Другие физические свойства воды, например, коэффициент поверхностного натяжения, число Прандтля и плотность уменьшаются при росте ее температуры. К примеру, плотность воды при нормальных условиях (20°С) имеет значение 998,2 кг/м 3 , а при температуре кипения снижается до 958,4 кг/м 3 .
Такое свойство воды, как теплопроводность (или правильнее — коэффициент теплопроводности) при нагревании имеет тенденцию к увеличению. Теплопроводность воды при температуре кипения 100°С достигает значения 0,683 Вт/(м·град). Температуропроводность H2O также увеличивается при росте ее температуры.
Следует отметить нелинейное поведение кривой зависимости удельной теплоемкости этой жидкости от температуры. Ее значение снижается в интервале от 0 до 40°С, затем происходит постепенный рост теплоемкости до величины 4220 Дж/(кг·град) при 100°С.
| t, °С → | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
|---|---|---|---|---|---|---|---|---|---|---|---|
| ρ, кг/м 3 | 999,8 | 999,7 | 998,2 | 995,7 | 992,2 | 988 | 983,2 | 977,8 | 971,8 | 965,3 | 958,4 |
| h, кДж/кг | 0 | 42,04 | 83,91 | 125,7 | 167,5 | 209,3 | 251,1 | 293 | 335 | 377 | 419,1 |
| Cp, Дж/(кг·град) | 4217 | 4191 | 4183 | 4174 | 4174 | 4181 | 4182 | 4187 | 4195 | 4208 | 4220 |
| λ, Вт/(м·град) | 0,569 | 0,574 | 0,599 | 0,618 | 0,635 | 0,648 | 0,659 | 0,668 | 0,674 | 0,68 | 0,683 |
| a·10 8 , м 2 /с | 13,2 | 13,7 | 14,3 | 14,9 | 15,3 | 15,7 | 16 | 16,3 | 16,6 | 16,8 | 16,9 |
| μ·10 6 , Па·с | 1788 | 1306 | 1004 | 801,5 | 653,3 | 549,4 | 469,9 | 406,1 | 355,1 | 314,9 | 282,5 |
| ν·10 6 , м 2 /с | 1,789 | 1,306 | 1,006 | 0,805 | 0,659 | 0,556 | 0,478 | 0,415 | 0,365 | 0,326 | 0,295 |
| β·10 4 , град -1 | -0,63 | 0,7 | 1,82 | 3,21 | 3,87 | 4,49 | 5,11 | 5,7 | 6,32 | 6,95 | 7,52 |
| σ·10 4 , Н/м | 756,4 | 741,6 | 726,9 | 712,2 | 696,5 | 676,9 | 662,2 | 643,5 | 625,9 | 607,2 | 588,6 |
| Pr | 13,5 | 9,52 | 7,02 | 5,42 | 4,31 | 3,54 | 2,93 | 2,55 | 2,21 | 1,95 | 1,75 |
Примечание: Температуропроводность в таблице дана в степени 10 8 , вязкость в степени 10 6 и т. д. для других свойств. Размерность физических свойств воды выражена в единицах СИ.
Теплофизические свойства воды на линии насыщения (100…370°С)
В таблице представлены теплофизические свойства воды H2O на линии насыщения в зависимости от температуры (в диапазоне от 100 до 370°С). Каждому значению температуры, при которой вода находится в состоянии насыщения, соответствует давление ее насыщенного пара. При этих параметрах жидкость и ее пар находятся в состоянии насыщения или термодинамического равновесия.
В таблице даны следующие теплофизические свойства воды в состоянии насыщенной жидкости:
- давление насыщенного пара при указанной температуре p, Па;
- плотность воды ρ, кг/м 3 ;
- удельная энтальпия воды h, кДж/кг;
- удельная (массовая) теплоемкость Cp, кДж/(кг·град);
- теплопроводность λ, Вт/(м·град);
- температуропроводность a, м 2 /с;
- вязкость динамическая μ, Па·с;
- вязкость кинематическая ν, м 2 /с;
- коэффициент теплового объемного расширения β, К -1 ;
- коэффициент поверхностного натяжения σ, Н/м;
- число Прандтля Pr.
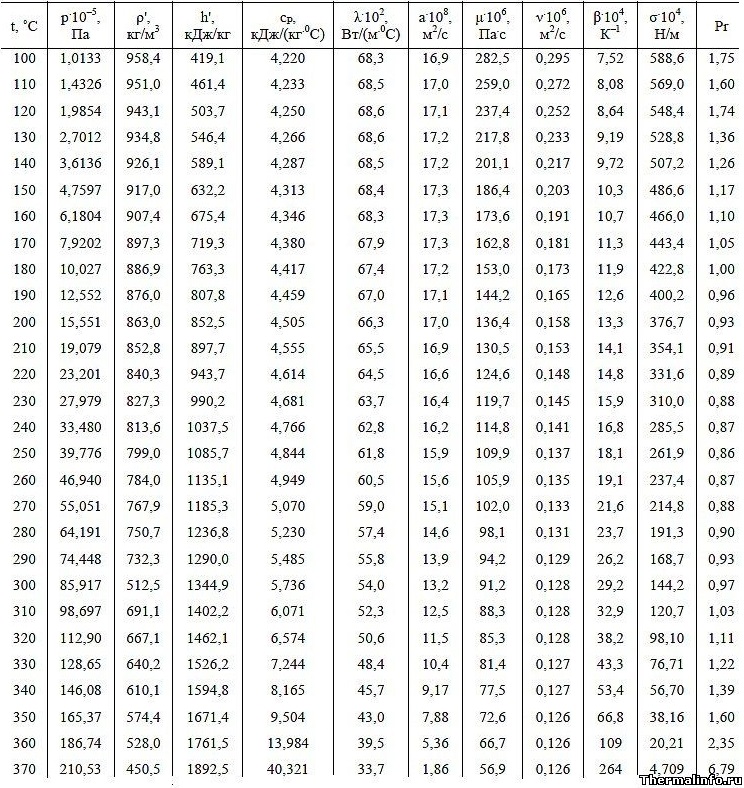
Свойства воды на линии насыщения имеют зависимость от температуры. Ее влияние особенно сказывается на вязкости воды — динамическая вязкость H2O при повышении температуры значительно снижается. Если, при температуре 100°С значение этого свойства воды в состоянии насыщения равно 282,5·10 -6 Па·с, то при температуре, равной, например 370°С, динамическая вязкость снижается до величины 56,9·10 -6 Па·с.
Другие свойства воды такие, как плотность, теплопроводность, удельная теплоемкость, температуропроводность при росте ее температуры имеют тенденцию к снижению своих значений. Например, плотность воды уменьшается с 958,4 до 450,5 кг/м 3 при нагревании со 100 до 370°С.
Теплопроводность воды в состоянии насыщения при увеличении температуры также снижается (в отличие от нормальных условий и температуре до 100°С, при которых имеет место ее рост в процессе нагрева). Снижение теплопроводности связано с увеличением как температуры, так и давления насыщенной жидкости.
Следует отметить, что удельная энтальпия воды в зависимости от температуры значительно увеличивается при нагревании, как до температуры кипения, так и выше.
Теплопроводность воды в зависимости от температуры при атмосферном давлении
В таблице представлены значения теплопроводности воды в жидком состоянии при нормальном атмосферном давлении. Теплопроводность воды указана в зависимости от температуры в интервале от 0 до 100°С.
Вода при нагревании становиться более теплопроводной — ее коэффициент теплопроводности увеличивается. Например, при 10°С вода имеет теплопроводность 0,574 Вт/(м·град), а при росте температуры до 95°С величина теплопроводности воды увеличивается до значения 0,682 Вт/(м·град).
Теплопроводность воды в зависимости от температуры и давления
В таблице приведены значения теплопроводности воды и водяного пара при температурах от 0 до 700°С и давлении от 1 до 500 атм.
Как известно, вода при атмосферном давлении закипает и переходит в пар при температуре 100°С. Коэффициент теплопроводности воды в этих условиях равен 0,683 Вт/(м·град). При увеличении давления растет и температура кипения воды (закон Клапейрона — Клаузиуса). По данным таблицы видно, при давлении в 100 раз выше атмосферного (100 бар) вода находится в виде пара при температуре от 310°С и имеет теплопроводность 0,523 Вт/(м·град).
Таким образом, следует отметить, что изменение давления влияет как на температуру кипения воды, так и на величину ее теплопроводности. Высокая теплопроводность воды достигается за счет роста давления — при повышении давления коэффициент теплопроводности воды увеличивается. Например, при давлении 1 бар и температуре 20°С вода имеет теплопроводность, равную 0,603 Вт/(м·град). При росте давления до 500 бар теплопроводность воды становится равной 0,64 Вт/(м·град) при этой же температуре.
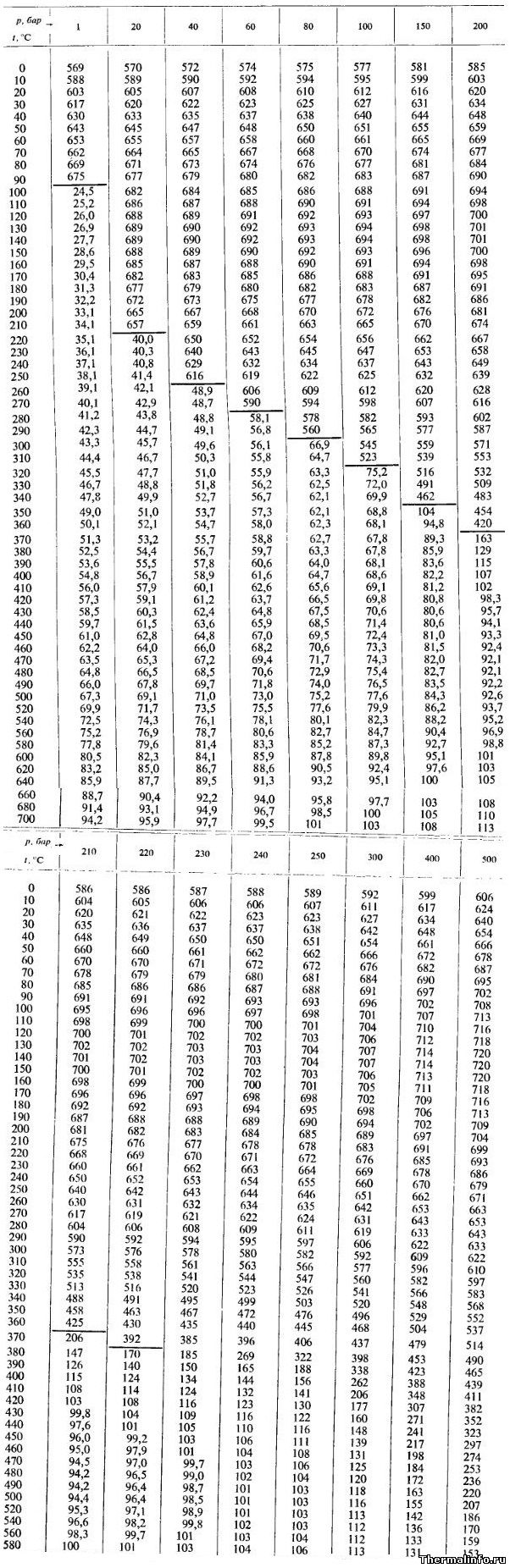
Примечание: Черта под значениями в таблице означает фазовый переход воды в пар, то есть цифры под чертой относятся к пару, а выше ее — к воде. Теплопроводность в таблице указана в степени 10 3 . Не забудьте разделить на 1000! Размерность теплопроводности воды в таблице Вт/(м·град).
В предыдущем параграфе мы рассматривали график плавления и отвердевания льда. Из графика видно, что, пока лёд плавится, температура его не меняется (см. рис. 18). И лишь после того, как весь лёд расплавится, температура образовавшейся жидкости начинает повышаться. Но ведь и во время процесса плавления лёд получает энергию от сгорающего в нагревателе топлива. А из закона сохранения энергии следует, что она не может исчезнуть. На что же расходуется энергия топлива во время плавления?

Переход металла в жидкое состояние при нагревании его до температуры плавления
Мы знаем, что в кристаллах молекулы (или атомы) расположены в строгом порядке. Однако и в кристаллах они находятся в тепловом движении (колеблются). При нагревании тела средняя скорость движения молекул возрастает. Следовательно, возрастает и их средняя кинетическая энергия и температура. На графике это участок АВ (см. рис. 18). Вследствие этого размах колебаний молекул (или атомов) увеличивается. Когда тело нагреется до температуры плавления, то нарушится порядок в расположении частиц в кристаллах. Кристаллы теряют свою форму. Вещество плавится, переходя из твёрдого состояния в жидкое.
Следовательно, вся энергия, которую получает кристаллическое тело после того, как оно уже нагрето до температуры плавления, расходуется на разрушение кристалла. В связи с этим температура тела перестаёт повышаться. На графике (см. рис. 18) это участок ВС.
Опыты показывают, что для превращения различных кристаллических веществ одной и той же массы в жидкость при температуре плавления требуется разное количество теплоты.
Физическая величина, показывающая, какое количество теплоты необходимо сообщить кристаллическому телу массой 1 кг, чтобы при температуре плавления полностью перевести его в жидкое состояние, называется удельной теплотой плавления.
Определяют удельную теплоту плавления на опыте. Так, было установлено, что удельная теплота плавления льда равна 3,4 • 10 5 — . Это означает, что для превращения куска льда массой 1 кг, взятого при 0 °С, в воду такой же температуры требуется затратить 3,4 • 10 5 Дж энергии. А чтобы расплавить брусок из свинца массой 1 кг, взятого при его температуре плавления, потребуется затратить 2,5 • 10 4 Дж энергии.
Следовательно, при температуре плавления внутренняя энергия вещества в жидком состоянии больше внутренней энергии такой же массы вещества в твёрдом состоянии.
Чтобы вычислить количество теплоты Q, необходимое для плавления кристаллического тела массой т, взятого при его температуре плавления и нормальном атмосферном давлении, нужно удельную теплоту плавления λ умножить на массу тела m:
Из этой формулы можно определить, что
λ = Q / m, m = Q / λ
Опыты показывают, что при отвердевании кристаллического вещества выделяется точно такое же количество теплоты, которое поглощается при его плавлении. Так, при отвердевании воды массой 1 кг при температуре 0 °С выделяется количество теплоты, равное 3,4 • 10 5 Дж. Точно такое же количество теплоты требуется и для плавления льда массой 1 кг при температуре 0 °С.

Превращение льда в воду
При отвердевании вещества всё происходит в обратном порядке. Скорость, а значит, и средняя кинетическая энергия молекул в охлаждённом расплавленном веществе уменьшаются. Силы притяжения теперь могут удерживать медленно движущиеся молекулы друг около друга. Вследствие этого расположение частиц становится упорядоченным — образуется кристалл. Выделяющаяся при кристаллизации энергия расходуется на поддержание постоянной температуры. На графике это участок EF (см. рис. 18).
Кристаллизация облегчается, если в жидкости с самого начала присутствуют какие-либо посторонние частицы, например пылинки. Они становятся центрами кристаллизации. В обычных условиях в жидкости имеется множество центров кристаллизации, около которых и происходит образование кристалликов.
Таблица 4.
Удельная теплота плавления некоторых веществ (при нормальном атмосферном давлении)

При кристаллизации происходит выделение энергии и передача её окружающим телам.
Количество теплоты, выделяющееся при кристаллизации тела массой т, определяется также по формуле
Внутренняя энергия тела при этом уменьшается.
Пример. Для приготовления чая турист положил в котелок лёд массой 2 кг, имеющий температуру 0 °С. Какое количество теплоты необходимо для превращения этого льда в кипяток при температуре 100 °С? Энергию, израсходованную на нагревание котелка, не учитывать.

Нагревание льда в котелке
Какое количество теплоты понадобилось бы, если вместо льда турист взял из проруби воду той же массы при той же температуре?
Переход вещества из твердого кристаллического состояния в жидкое называется плавлением. Чтобы расплавить твердое кристаллическое тело, его нужно нагреть до определенной температуры, т. е. подвести тепло. Температура, при которой вещество плавится, называется температурой плавления вещества.
Обратный процесс — переход из жидкого состояния в твердое — происходит при понижении температуры, т. е. тепло отводится. Переход вещества из жидкого состояния в твердое называется отвердеванием, или кристаллизацией. Температура, при которой вещество кристаллизуется, называется температурой кристаллизации.
Опыт показывает, что любое вещество кристаллизуется и плавится при одной и той же температуре.
На рисунке представлен график зависимости температуры кристаллического тела (льда) от времени нагревания (от точки А до точки D) и времени охлаждения (от точки D до точки K). На нем по горизонтальной оси отложено время, а по вертикальной — температура.

Из графика видно, что наблюдение за процессом началось с момента, когда температура льда была -40 °С, или, как принято говорить, температура в начальный момент времени tнач = -40 °С (точка А на графике). При дальнейшем нагревании температура льда растет (на графике это участок АВ). Увеличение температуры происходит до 0 °С — температуры плавления льда. При 0°С лед начинает плавиться, а его температура перестает расти. В течение всего времени плавления (т.е. пока весь лед не расплавится) температура льда не меняется, хотя горелка продолжает гореть и тепло, следовательно, подводится. Процессу плавления соответствует горизонтальный участок графика ВС. Только после того как весь лед расплавится и превратится в воду, температура снова начинает подниматься (участок CD). После того, как температура воды достигнет +40 °С, горелку гасят и воду начинают охлаждать, т. е. тепло отводят (для этого можно сосуд с водой поместить в другой, больший сосуд со льдом). Температура воды начинает снижаться (участок DE). При достижении температуры 0 °С температура воды перестает снижаться, несмотря на то, что тепло по-прежнему отводится. Это идет процесс кристаллизации воды — образования льда (горизонтальный участок EF). Пока вся вода не превратится в лед, температура не изменится. Лишь после этого начинает уменьшаться температура льда (участок FK).
Вид рассмотренного графика объясняется следующим образом. На участке АВ благодаря подводимому теплу средняя кинетическая энергия молекул льда увеличивается, и температура его повышается. На участке ВС вся энергия, получаемая содержимым колбы, тратится на разрушение кристаллической решетки льда: упорядоченное пространственное расположение его молекул сменяется неупорядоченным, меняется расстояние между молекулами, т.е. происходит перестройка молекул таким образом, что вещество становится жидким. Средняя кинетическая энергия молекул при этом не меняется, поэтому неизменной остается и температура. Дальнейшее увеличение температуры расплавленного льда-воды (на участке CD) означает увеличение кинетической энергии молекул воды вследствие подводимого горелкой тепла.
При охлаждении воды (участок DE) часть энергии у нее отбирается, молекулы воды движутся с меньшими скоростями, их средняя кинетическая энергия падает — температура уменьшается, вода охлаждается. При 0°С (горизонтальный участок EF) молекулы начинают выстраиваться в определенном порядке, образуя кристаллическую решетку. Пока этот процесс не завершится, температура вещества не изменится, несмотря на отводимое тепло, а это означает, что при отвердевании жидкость (вода) выделяет энергию. Это как раз та энергия, которую поглотил лед, превращаясь в жидкость (участок ВС). Внутренняя энергия у жидкости больше, чем у твердого тела. При плавлении (и кристаллизации) внутренняя энергия тела меняется скачком.
Металлы, плавящиеся при температуре выше 1650 ºС, называют тугоплавкими (титан, хром, молибден и др.). Самая высокая температура плавления среди них у вольфрама — около 3400 °С. Тугоплавкие металлы и их соединения используют в качестве жаропрочных материалов в самолетостроении, ракетостроении и космической технике, атомной энергетике.
Подчеркнем еще раз, что при плавлении вещество поглощает энергию. При кристаллизации оно, наоборот, отдает ее в окружающую среду. Получая определенное количество теплоты, выделяющееся при кристаллизации, среда нагревается. Это хорошо известно многим птицам. Недаром их можно заметить зимой в морозную погоду сидящими на льду, который покрывает реки и озера. Из-за выделения энергии при образовании льда воздух над ним оказывается на несколько градусов теплее, чем в лесу на деревьях, и птицы этим пользуются.
Плавление аморфных веществ .
Наличие определенной точки плавления — это важный признак кристаллических веществ. Именно по этому признаку их можно легко отличить от аморфных тел, которые также относят к твердым телам. К ним, в частности, относятся стекла, очень вязкие смолы, пластмассы.
Аморфные вещества (в отличие от кристаллических) не имеют определенной температуры плавления — они не плавятся, а размягчаются. При нагревании кусок стекла, например, сначала становится из твердого мягким, его легко можно гнуть или растягивать; при более высокой температуре кусок начинает менять свою форму под действием собственной тяжести. По мере нагревания густая вязкая масса принимает форму того сосуда, в котором лежит. Эта масса сначала густая, как мед, затем — как сметана и, наконец, становится почти такой же маловязкой жидкостью, как вода. Однако указать определенную температуру перехода твердого тела в жидкое здесь невозможно, поскольку ее нет.
Теплота плавления .
Теплота плавления — это количество теплоты, которое необходимо сообщить веществу при постоянном давлении и постоянной температуре, равной температуре плавления, чтобы полностью перевести его из твердого кристаллического состояния в жидкое. Теплота плавления равна тому количеству теплоты, которое выделяется при кристаллизации вещества из жидкого состояния. При плавлении вся подводимая к веществу теплота идет на увеличение потенциальной энергии его молекул. Кинетическая энергия не меняется, поскольку плавление идет при постоянной температуре.
Изучая на опыте плавление различных веществ одной и той же массы, можно заметить, что для превращения их в жидкость требуется разное количество теплоты. Например, для того чтобы расплавить один килограмм льда, нужно затратить 332 Дж энергии, а для того чтобы расплавить 1 кг свинца — 25 кДж.
Физическая величина, показывающая, какое количество теплоты необходимо сообщить кристаллическому телу массой 1 кг, чтобы при температуре плавления полностью перевести его в жидкое состояние, называется удельной теплотой плавления.
Удельную теплоту плавления измеряют в джоулях на килограмм (Дж/кг) и обозначают греческой буквой λ (лямбда).
Удельная теплота кристаллизации равна удельной теплоте плавления, поскольку при кристаллизации выделяется такое же количество теплоты, какое поглощается при плавлении. Так, например, при замерзании воды массой 1 кг выделяются те же 332 Дж энергии, которые нужны для превращения такой же массы льда в воду.
Чтобы найти количество теплоты, необходимое для плавления кристаллического тела произвольной массы, или теплоту плавления, надо удельную теплоту плавления этого тела умножить на его массу:
Теплота сгорания .
Теплота сгорания (или теплотворная способность, калорийность) — это количество теплоты, выделяющейся при полном сгорании топлива.
Для нагревания тел часто используют энергию, выделяющуюся при сгорании топлива. Обычное топливо (уголь, нефть, бензин) содержит углерод. При горении атомы углерода соединяются с атомами кислорода, содержащегося в воздухе, в результате чего образуются молекулы углекислого газа. Кинетическая энергия этих молекул оказывается большей, чем у исходных частиц. Увеличение кинетической энергии молекул в процессе горения называют выделением энергии. Энергия, выделяющаяся при полном сгорании топлива, и есть теплота сгорания этого топлива.
Теплота сгорания топлива зависит от вида топлива и его массы. Чем больше масса топлива, тем больше количество теплоты, выделяющейся при его полном сгорании.
Физическая величина, показывающая, какое количество теплоты выделяется при полном сгорании топлива массой 1 кг, называется удельной теплотой сгорания топлива. Удельную теплоту сгорания обозначают буквой q и измеряют в джоулях на килограмм (Дж/кг).
Количество теплоты Q, выделяющееся при сгорании m кг топлива, определяют по формуле:
Чтобы найти количество теплоты, выделяющееся при полном сгорании топлива произвольной массы, нужно удельную теплоту сгорания этого топлива умножить на его массу.

Здоровье
Модель строения воды
Молекула воды включает два атома водорода (Н) и один атом кислорода (О). Элементы, из которых состоит жидкость, определяют всю функциональность и особенности. Модель молекулы воды имеет форму треугольника. Вершину этой геометрической фигуры представляет крупный элемент кислорода, а внизу находятся небольшие атомы водорода.
Молекула воды обладает двумя положительными и двумя отрицательными полюсами зарядов. Отрицательные заряды формируются из-за излишка электронной плотности у атомов кислорода, а положительные – из-за нехватки электронной плотности у водорода.

Неравномерное распределение электрических зарядов создает диполе, где диполярный момент составляет 1,87 дебай. Вода обладает способностью растворять вещества, поскольку ее молекулы пытаются нейтрализовать электрическое поле. Диполя приводят к тому, что на поверхности погруженных в жидкость веществ становятся слабее межатомные и межмолекулярные связи.
Вода отличает большой устойчивостью при растворении прочих соединений. В обычных условиях из 1 млрд молекул только 2 распадаются, а протон переходит в строение иона гидроксония (образуется при растворении кислот).
Вода не меняет свой состав при взаимодействии с другими веществами и не влияет на структуру этих соединений. Такая жидкость считается инертным растворителем, что особо важно для живых организмов. Полезные вещества поступают к различным органам через водные растворы, поэтому важно, чтобы их состав и свойства оставались неизменными. Вода сохраняет в себе память о растворенных в ней веществах и может применяться многократно.
Каковы особенности пространственной организации молекулы воды:
- Соединение проводится противоположными зарядами;
- Появляются межмолекулярные водородные связи, которые исправляют электронную неполноценность водорода с помощью дополнительной молекулы;
- Вторая молекула фиксирует водород по отношению к кислороду;
- Благодаря этому образуются четыре водородные связи, которые могут контактировать с 4 соседями;
- Такая модель напоминает бабочку и имеет углы равные 109 градусам.
Атомы водорода соединяются с атомами кислорода и образуют молекулу воды с ковалентной связью. Водородные соединения более сильные, поэтому, когда они разрываются, то молекулы присоединяются к другим веществам, способствуя их растворению.
Прочие химические элементы, в состав которых входит водород, замерзают при -90 градусах, а закипают при 70 градусах. Но вода становится льдом, когда температура достигает нуля, а закипает при 100 градусах. Чтобы объяснить такие отклонения от нормы, требуется разобраться, в чем особенность строения молекулы воды. Дело в том, что вода – это ассоциированная жидкость.

Это свойство подтверждается и большой теплотой парообразования, что делает жидкость хорошим энергоносителем. Вода – отличный регулятор температуры, способен нормализировать резкие перепады этого показателя. Теплоемкость жидкости повышается, когда ее температура 37 градусов. Минимальные показатели соответствуют температуре человеческого тела.
Относительная молекулярная масса воды составляет 18. Рассчитать этот показатель достаточно легко. Следует заранее ознакомиться с атомной массой кислорода и водорода, которая равна 16 и 1 соответственно. В химических задачах нередко встречается массовая доля воды. Этот показатель измеряется в проценте и зависит от формулы, которую требуется рассчитать.
Строение молекулы в различных агрегатных состояниях воды
В жидком состоянии молекула воды состоит из моногидроля, дигидроля и тригидроля. Количество этих элементов зависит от агрегатного состояния жидкости. Пар включает одну H₂O – гидроль (моногидроль). Две H₂O обозначают жидкое состояние – дигидроль. Три H₂O включает лед.
Агрегатные состояния воды:
- Жидкое. Между одиночными молекулами, которые связаны водородными связями, располагаются пустоты.
- Пар. Одиночные H₂O никак не соединяются между собой.
- Лед. Твердое состояние отличается прочными водородными связи.
При этом существуют переходные состояния жидкости, например, при испарении или замерзании. Для начала требуется разобраться, отличаются ли молекулы воды от молекул льда. Так замерзшая жидкость имеет кристаллическую структуру. Модель льда может иметь форму тетраэдр, тригональной и моноклинной сингонии, куба.
Обычная и замерзшая вода отличаются плотностью. Кристаллическая структура приводит к меньшей плотности и увеличению объема. Основное различие между жидким и твердым состоянием – это количество, сила и разновидность водородных связей.
Состав не меняется ни в одном агрегатном состоянии. Отличается строение и движение составных частей жидкости, сила связей водорода. Обычно молекулы воды слабо притягиваются друг к другу, размещаются хаотично, поэтому жидкость такая текучая. Лед отличается более сильным притяжением, так как создается плотная кристаллическая решетка.
Многих интересует, одинаковы ли объемы и состав молекул холодной и горячей воды. Важно запомнить, что состав жидкости не меняется ни в одном из агрегатных состояний. Молекулы при нагревании или остывании жидкости отличаются расположением. В холодной и горячей воде разные объемы, так как в первом случае структура упорядоченная, а во втором – хаотичная.
Когда лед тает, то его температура не меняется. Только после того, как жидкость меняется свое агрегатное состояние, показатели начинают подниматься. Для таяния требуется определенное количество энергии, которое называется удельной теплотой плавления или лямбда воды. Для льда показатель равен 25000 Дж/кг.
Твердое состояние воды
Вода в твердом состоянии – это лёд и снег. Некоторые не понимают, к какому агрегатному состоянию воды относится иней. Конечно, к твёрдому! Это мелкая ледяная крошка, замерзшие капли росы.
Твердая – это замороженная вода. Когда она замерзает, ее молекулы отодвигаются подальше друг от друга, делая лед менее плотным, чем жидкость, т.е. вода в твердом состоянии занимает больший объем, чем в жидком.
Большинство веществ при снижении температуры сжимается, а вода – расширяется, и в этом ее уникальная особенность.
Замерзает – это значит, что при 0 градусов Цельсия вода кристаллизуется и переходит из жидкого состояния в твердое. Наличие в воде солей снижает температуру замерзания.
На школьных олимпиадах встречается такой интересный вопрос: какой металл, находясь в расплавленном состоянии, может заморозить воду? Ответ – ртуть, которая начинает плавиться при температуре -39 градусов Цельсия. Понятно, что жидкая ртуть при температуре от -38 до 0 способна заморозить воду, отбирая у нее тепло.
Несмотря на то, что самое распространенное на нашей планете — жидкое состояние воды, значительная ее часть (2/3 всех пресноводных запасов) находится в замороженном виде. Площадь ледников – около 11% всей суши Земли.
Если жидкое состояние пресной воды переходит в твердое при 0 градусов Цельсия, то морская вода средней солености замерзает примерно при -1,8 градусах Цельсия.
Жидкое состояние воды
Вода в жидком состоянии встречается на нашей планете не только в реках и океанах. Облака состоят из крошечных капелек воды и кристалликов льда, и дождь – это тоже жидкая вода.
Также вода в жидком состоянии просачивается через почву и образует подземные водные горизонты, из которых черпается основная масса питьевой воды.

Жидкая вода легко переходит в твердое и газообразное состояние. Главным образом, это зависит от температуры. Но свою роль играет и давление.
Физический переход воды из жидкого состояния в газообразное называется испарением, потому что газообразное состояние воды называется паром.
Как жидкое состояние воды превращается в газообразное? Когда мы кипятим воду, она превращается из жидкости в газ, или водяной пар. Когда его часть остывает, мы видим небольшое облако, которое и называют паром. Хотя, если мы его видим, то это уже жидкое состояние воды, т.е. скопление ее микроскопических капелек.
Закипает жидкая пресная вода при 100°C (градусах Цельсия) или 212°F (градусах Фарингейта), в условиях нормального атмосферного давления. Чем ниже давление (например, в горах), тем выше температура кипения.
Состояние газа
Итак, вода в газообразном состоянии – это пар. Утверждение, что большая часть воды в гидросфере находится в газообразном состоянии – не верно.
Не все хорошо себе представляют, в каком состоянии вода способна испаряться. Оказывается, вода в твердом состоянии испаряется так же, как и жидкая, только медленнее! Скорость испарения зависит от температуры. Т.е. в газообразное состояние вода может переходить прямо из твердого, минуя жидкое.

Испаренная с поверхности Земли вода в газообразном состоянии образует облака и тучи
Агрегатные состояния воды — переходные процессы
Процессы перехода воды с одного агрегатного состояния в другое определяются следующим образом:
- Кипение и парообразование — переход воды из жидкого состояния в пар;
- Конденсация — процесс перехода пара в жидкое состояние воды;
- Кристаллизация — переход жидкости в лед;
- Плавление – переход льда в жидкость;
- Сублимация – переход льда прямо в парообразное состояние;
- Десублимация – переход пара сразу в лед, примером может служить иней.
Граничные точки перехода воды в состояния лед/вода и вода/пар определили соответственно как 0 и 100 градусов по Цельсию при условии атмосферного давления 760 мм рт. ст. или 101 325 Па. Всем с детства хорошо известна простая примета, температура за окном опустилась ниже нуля, ждите снега 🙂
Вода всегда вокруг нас
Водный баланс – это основа жизни на нашей планете. Большая её часть на Земле – это океаны и моря. В них сосредоточено 97% данного вещества. Остальные 3 % – это реки, озёра, пруды, подземные воды и парообразная вода в атмосфере. Растения и животные для обеспечения своей жизнедеятельности ежедневно потребляют живительную влагу.
Вода – это составляющая часть организма человека. Каждая наша клетка больше чем наполовину состоит из этой жидкости. Кровь, текущая в наших венах, – это на 82% вода. Мышцы и кожа содержат её 76%. Удивительно, но даже кости в своём составе имеют до 30% воды. Её наименьшее содержание в зубной эмали – всего 0,3%.
Общая масса воды на планете Земля – более 2 000 000 000 миллионов тонн.

Какие существуют 3 состояния воды в природе?
Вода бывает в трёх состояниях:
- жидкая форма;
- парообразное состояние;
- твёрдая агрегатная форма — лёд.
Лёд – вода в твёрдом виде
Н2О из жидкого переходит в твёрдое агрегатное состояние при снижении температуры ниже 0 градусов по Цельсию. Интересно то, что почти все предметы при охлаждении уменьшаются в объёмах, а вода, наоборот, замерзая, расширяется. Если так она прозрачная и бесцветная, то при замерзании может приобретать белый цвет из-за попадания частичек воздуха внутрь льда.
Необычно, что при одной и той же кристаллической структуре лёд может иметь множество разнообразных форм. Твёрдое состояние воды в природе — это гигантские айсберги, блестящая корка льда на реке, белые хлопья снега, сосульки, висящие на крышах.
Лёд имеет огромное значение для хозяйственной деятельности человека и оказывает большое влияние на поддержание жизнедеятельности многих организмов. Например, при замерзании реки он выполняет защитную функцию, сохраняя водоём от дальнейшего промерзания, этим самым оберегая подводный мир.

Но также лёд может стать причиной разрушительных стихийных бедствий. Например, град, обледенение зданий и летательных аппаратов, промерзание почвы, ледяные обвалы.
В быту мы используем замёрзшую воду как хладагент, бросая небольшие кубики льда в напитки для их охлаждения. Подобным образом могут охлаждаться пищевые продукты и медицинские препараты.
Химические названия
- монооксид дигидрофосфата;
- гидроксильная кислота;
- дигидромонооксид
- оксидан

Происхождение воды на планете
Возникновение воды на нашей планете является предметом научных споров. Существует 2 основные гипотезы:
- Космическое происхождение. Часть учёных считают, что вода появилась вследствие падающих метеоритов, астероидов, которые содержали воду.
- Земное происхождение. Другие учёные считают, что вода образовалась на Земле во время формирования, а не занесена с космоса.
Образование воды
Многих интересует, какая вода находится в реках, морях, под землей. Образовавшаяся миллиарды лет назад вода сконцентрировалась в океанах. Из океанов она испаряется и поднимается, где образуются облака. После долгого путешествия она возвращается на землю в виде осадков. Вода собирается и возвращается через реки обратно в море. Часть просачивается в почву и попадает в грунтовые воды. Там формируются новые источники, которые текут в море.
В более холодном климате вода остается на ледниках, которые очень медленно, стекают к более низким высотам, где и тают. В полярных регионах этот механизм скольжения настолько медленный, что в ледниках можно найти воду, попавшую на поверхность Земли десятки тысяч лет назад. Вот откуда берется в природе вода.
Наука о воде
Изучением природных вод, явлений и процессов занимается наука Гидрология.
Первые упоминания о гидрологии появились на заре истории человечества около 6000 лет назад.
Начало гидрологических наблюдений в России относится к XV–XVI вв.: в записях русских летописцев сохранились сведения о свойствах воды, наводнениях, паводках, замерзании.
Значение на Земле
Без воздуха человек может прожить несколько секунд, без еды – несколько месяцев, без воды – максимум несколько суток. Снижение содержания воды в организме всего лишь на 2% может вызвать сильную слабость. При нехватке 8% уже может возникнуть серьезное недомогание, а при 12% – смерть.
Каждая клетка живого организма состоит из жидкости и нуждается в регулярном пополнении. Без воды не проживут ни люди, ни растения, ни животные.
Вода формирует климат, участвует в круговороте воды в природе, для многих живых организмов является средой обитания.
Эмпирическое правило Клечковского
Органолептические свойства воды
Сюда относятся показатели, которые возможно определить органами чувств. К ним относятся вкус, запах, цвет (цветность), мутность (прозрачность или непрозрачность). Часть параметров определяется не только с помощью носа, глаз, языка, но и на аналитическом оборудовании. Например, мутность и цветность определяют используя фотометр, а прозрачность — цилиндр и градировочную шкалу.
Характеризует вкусовые ощущения от попадания жидкости на рецепторы языка. Оценивается в баллах. иногда добавляют описание вкуса, помогающее оценить пригодность для питья, содержание специфических химических веществ.
Запах
Оценивает ощущения от вдыхания пара, образующегося над сосудом, содержащим исследуемую жидкость, через нос. Запах выражают баллами, которые характеризуют интенсивность запаха, а также указывают его характер, например:
- цветочный
- специфичный химический
- болотный
- затхлый
- свежести
- гнилостный
Выделяют специфические запахи химических соединений, например, хлора, сероводорода, фенола. По этой причине определение запаха предшествует определению других компонентов, помогает рассчитать коэффициент разбавления, скорректировать подготовку проб. Определять запах могут только сотрудники, прошедшие специальное обучение. Среди требований к помещению числится обеспечение отсутствия мешающих воздействий, включая цвет стен, а также отсутствие посторонних запахов.
Погрешность определению запаха добавляет использование неправильной тары для отбора. К ней относятся бутылки из-под газированных, ароматизированных напитков. Даже если тщательно вымыть такую тару запах все равно сохранится.
Цветность воды
Определяет изменение длины волны светового луча при прохождении через толщу раствора. Проще говоря, сосуд прямоугольной формы (длина большей стороны 1 или 5 сантиметров) заполняют исследуемым раствором, пропускают через него свет, изучают изменение этого света. Исследование проводят на оптическом приборе — фотометре или спектрофотометре. При проведении экспресс-анализа используют сравнение с стандартной шкалой. Это быстро, но не точно.
Мутность
Показывает содержание едва заметных взвешенных частиц, которые снижают способность раствора пропускать свет. Это происходит за счет того, что взвесь отражает, рассеивает часть света, проходящего через слой жидкости. Мутность определяют экспресс-методом используя цилиндр с прозрачным дном и бумагу с нанесенным стандартным шрифтом. При таком определении параметр могут называть прозрачностью по шрифту. Мутность не выявляет конкретный компонент, то есть определить характер взвеси определяя только этот параметр невозможно. Он выявляет присутствие посторонних частиц, служит показанием к проведению дополнительных анализов или установке механического фильтра.
Читайте также:

